Alat kesehatan memainkan peran penting dalam pelayanan kesehatan dengan menyediakan fungsi diagnostik, preventif, terapeutik, pemantauan, atau rehabilitatif. Di Indonesia, alat kesehatan diatur oleh Kementerian Kesehatan (Kemenkes), yang menjamin keamanan, efikasi, dan mutunya. Kerangka regulasi mengategorikan alat kesehatan ke dalam beberapa kelas berdasarkan risiko, yang menentukan proses regulasi, persyaratan registrasi, dan pengawasan. Artikel ini memberikan tinjauan mendalam mengenai klasifikasi ini, kriteria untuk masing-masing klasifikasi, dan proses registrasi terkait di Indonesia.
Klasifikasi Alat Kesehatan di Indonesia
Alat kesehatan Klasifikasi di Indonesia sangat penting dalam menentukan kerangka regulasi untuk berbagai alat kesehatan berdasarkan risiko yang terkait. Sistem ini selaras dengan pedoman internasional, termasuk Global Harmonization Task Force (GHTF) dan ASEAN Medical Devices Directive (AMDD), untuk memastikan harmonisasi global sekaligus mengakomodasi kebutuhan lokal. Klasifikasi ke dalam Kelas I, II, dan III ini bukan sekadar kategorisasi, melainkan aspek mendasar yang memengaruhi keseluruhan proses regulasi, termasuk kompleksitas registrasi, pengawasan yang diterapkan, dan biaya terkait. Setiap klasifikasi menetapkan persyaratan regulasi yang spesifik, memastikan bahwa alat kesehatan dievaluasi secara tepat untuk keamanan dan efikasi berdasarkan profil risikonya.
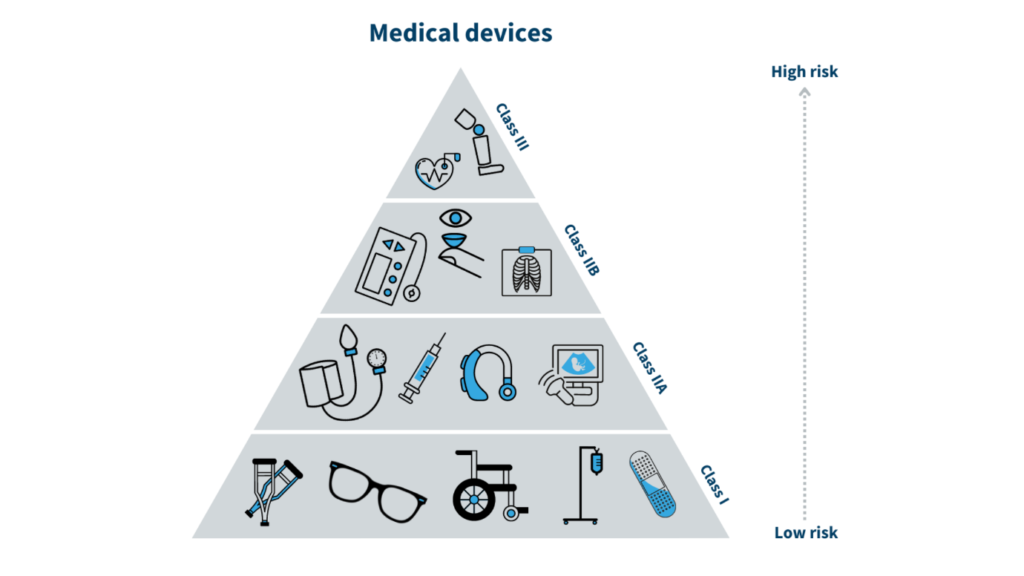
Kelas I (Perangkat Berisiko Rendah)
Perangkat Kelas I adalah yang paling sederhana di antara ketiga klasifikasi, yang menunjukkan risiko minimal bagi pengguna. Perangkat ini umumnya tidak memerlukan kondisi steril atau pemantauan khusus agar aman dan efektif. Contoh umum perangkat Kelas I meliputi perban sederhana, stetoskop non-pengukur, kruk, dan sarung tangan bedah. Kriteria untuk klasifikasi ini berfokus pada profil risiko rendah dari perangkat ini. Perangkat ini non-invasif, yang berarti tidak memasuki tubuh atau menembus kulit dan tidak memerlukan pengukuran langsung untuk berfungsi dengan baik. Persyaratan peraturan untuk perangkat Kelas I relatif mudah. Proses pendaftaran disederhanakan, biasanya memakan waktu sekitar 15 hari, dan melibatkan dokumentasi minimal, yang meliputi pelabelan perangkat, informasi produsen, dan analisis risiko dasar. Biaya terkait untuk mendaftarkan perangkat Kelas I juga lebih rendah, yaitu sekitar Rp1.500.000 (US$115).
Kelas II (Perangkat Risiko Sedang)
Beralih ke Kelas II, perangkat-perangkat ini dianggap memiliki risiko yang lebih tinggi dibandingkan Kelas I, sehingga memerlukan pengawasan regulasi yang lebih ketat. Perangkat-perangkat ini meliputi pompa infus, mesin EKG, mesin sinar-X, dan mesin anestesi. Kriteria untuk perangkat Kelas II mencerminkan risiko kesehatan sedang, karena bersifat invasif atau dapat bersentuhan langsung dengan pengguna, sehingga memerlukan pemantauan yang cermat dan terkadang sterilisasi. Persyaratan regulasi untuk perangkat Kelas II mencakup proses registrasi yang lebih komprehensif, biasanya memakan waktu sekitar 30 hari. Proses ini melibatkan penilaian terperinci yang mencakup laporan evaluasi klinis, dokumen manajemen risiko, dan sertifikat Cara Pembuatan Obat yang Baik (CPOB). Biaya terkait lebih tinggi, sekitar Rp3.000.000 (US$$230), yang mencerminkan peningkatan pengawasan dan tuntutan regulasi terhadap perangkat ini.
Kelas III (Perangkat Berisiko Tinggi)
Kelas III mewakili kategori risiko tertinggi, diperuntukkan bagi perangkat yang dapat menyebabkan cedera serius atau kematian jika tidak berfungsi. Ini termasuk perangkat implan seperti alat pacu jantung, defibrilator, dan prostetik. Kriteria untuk perangkat Kelas III berfokus pada sifatnya yang berisiko tinggi, karena biasanya dapat ditanamkan atau menyediakan pengukuran penting yang diperlukan untuk keputusan terapeutik. Persyaratan peraturan untuk perangkat ini adalah yang paling ketat, dengan proses registrasi memakan waktu hingga 45 hari. Kategori ini menuntut dokumentasi yang komprehensif, termasuk uji klinis, studi biokompatibilitas, dan laporan evaluasi klinis. Biaya registrasi untuk perangkat Kelas III juga yang tertinggi, sekitar Rp5.000.000 (US$340), yang mencerminkan pentingnya perangkat ini bagi keselamatan pasien. Persyaratan yang ketat memastikan bahwa hanya perangkat dengan keamanan dan efikasi yang terbukti yang disetujui untuk digunakan di Indonesia.
Proses Registrasi Alat Kesehatan di Indonesia
Proses registrasi alat kesehatan di Indonesia melibatkan prosedur multi-tahap yang dirancang untuk memastikan keamanan, efikasi, dan kualitas alat kesehatan tersebut sebelum dapat dipasarkan secara legal. Prosesnya bervariasi tergantung klasifikasi alat kesehatan (Kelas I, II, atau III), dan masing-masing memiliki persyaratannya sendiri. Memahami langkah-langkah ini sangat penting bagi produsen yang ingin memasuki pasar Indonesia, karena langkah-langkah ini menentukan dokumentasi yang dibutuhkan serta jangka waktu dan biaya yang terkait dengan setiap kategori alat kesehatan.
Registrasi Pra-pasar
Prosesnya dimulai dengan mengirimkan formulir aplikasi ke Kementerian Kesehatan (Kemenkes) melalui importir atau distributor lokal berlisensi. Formulir ini harus mencakup informasi lengkap tentang perangkat, seperti tujuan penggunaannya, spesifikasi desain, dan evaluasi klinis. Pemohon harus memberikan ringkasan eksekutif yang menguraikan tujuan dan manfaat perangkat serta informasi pelabelan terperinci, termasuk petunjuk penggunaan, kontraindikasi, peringatan, dan tindakan pencegahan. Selain itu, pengajuan tersebut memerlukan detail produsen, termasuk sertifikasi ISO 13485, standar untuk manajemen mutu dalam perangkat medis, yang menunjukkan kepatuhan terhadap praktik terbaik internasional dalam manufaktur. Analisis risiko sangat penting dalam mengevaluasi potensi risiko yang terkait dengan penggunaan perangkat. Laporan evaluasi klinis berdasarkan uji klinis dan studi yang menunjukkan keamanan dan efikasi juga diperlukan. Selain itu, Sertifikat Penjualan Bebas (FSC) dari negara produsen, yang menyatakan bahwa perangkat tersebut dijual bebas di sana, diperlukan untuk menunjukkan penerimaan perangkat di pasar internasional. Dokumentasi pengujian biokompatibilitas harus disediakan, yang menunjukkan bahwa bahan perangkat aman untuk digunakan manusia. Biaya pendaftaran bervariasi berdasarkan klasifikasi perangkat; Perangkat Kelas I memerlukan biaya lebih rendah, sekitar Rp1.500.000 (US$115). Perangkat Kelas II dan III memerlukan biaya lebih tinggi karena kompleksitas dan persyaratan dokumentasi yang lebih tinggi.
Registrasi Pasca-Pasar
Setelah Kementerian Kesehatan mengevaluasi semua dokumen yang diajukan dan melakukan penilaian risiko, lisensi produk dan nomor registrasi akan diterbitkan. Pemegang lisensi harus merupakan entitas lokal, baik importir maupun distributor, yang wajib mempertahankan registrasi tersebut. Masa berlaku lisensi produk biasanya berkisar antara 2 hingga 5 tahun, tergantung pada jenis alat kesehatan dan Surat Kuasa (SKK). Perpanjangan lisensi diperlukan sebelum masa berlakunya habis agar alat kesehatan dapat terus dipasarkan secara legal di Indonesia. Fase pasca-pemasaran ini krusial untuk menjaga kepatuhan terhadap standar regulasi, terutama jika terdapat perubahan pada kemasan, label, atau spesifikasi teknis alat kesehatan. Permohonan amandemen dapat diajukan untuk perubahan kecil, sementara modifikasi besar mungkin memerlukan registrasi baru. Entitas lokal bertanggung jawab untuk memastikan bahwa semua pembaruan dan amandemen segera dikomunikasikan kepada Kementerian Kesehatan, menjaga kepatuhan alat kesehatan selama siklus hidupnya di pasar. Pengawasan regulasi pasca-registrasi ini dirancang untuk memastikan keamanan dan efikasi yang berkelanjutan, yang memungkinkan Kementerian Kesehatan untuk memantau efek samping dan melakukan pembaruan yang diperlukan terhadap spesifikasi produk sesuai kebutuhan.
Registrasi E-Katalog di Indonesia
Pengenalan sistem e-Katalog oleh pemerintah Indonesia menandai perubahan penting dalam cara alat kesehatan terdaftar dan dibeli. Platform daring ini memungkinkan alat kesehatan terdaftar untuk didaftarkan dan diakses oleh penyedia layanan kesehatan dan entitas pengadaan pemerintah, sehingga menyederhanakan proses pengadaan. Pencantuman alat kesehatan dalam e-Katalog melibatkan evaluasi menyeluruh untuk memastikan alat kesehatan tersebut memenuhi standar dan persyaratan peraturan khusus yang ditetapkan oleh Kementerian Kesehatan (Kemenkes). Setelah mendapatkan izin produk, alat kesehatan tersebut dapat diunggah ke e-Katalog melalui importir lokal berlisensi. Proses ini memerlukan penyerahan dokumentasi yang diperlukan, seperti ringkasan eksekutif, informasi pelabelan terperinci, analisis risiko, dan laporan evaluasi klinis. Untuk memastikan keamanan dan efikasi, alat kesehatan harus mematuhi standar manajemen mutu setempat, termasuk sertifikasi ISO 13485.

Manfaat mendaftarkan perangkat di e-Katalog sangat beragam. Hal ini mengurangi beban administratif bagi produsen dan penyedia layanan kesehatan dengan menggabungkan proses pengadaan ke dalam satu platform digital. Hal ini mempercepat proses pembelian dan menurunkan biaya pengadaan melalui peningkatan persaingan pemasok. Selain itu, sistem e-Katalog meningkatkan transparansi, sehingga memudahkan perbandingan perangkat berdasarkan spesifikasi teknis, harga, dan catatan keamanannya. Bagi produsen, terdaftar di e-Katalog dapat meningkatkan akses dan visibilitas pasar secara signifikan, terutama bagi entitas asing. Hal ini menyediakan lokasi terpusat di mana lembaga pemerintah dapat dengan cepat mengidentifikasi dan menyediakan perangkat yang dibutuhkan, sehingga meningkatkan kualitas layanan kesehatan di Indonesia secara keseluruhan.
Tantangan dan Pertimbangan Registrasi Alat Kesehatan di Indonesia
Terlepas dari kelebihannya, sistem e-Katalog juga menghadirkan tantangan yang harus dihadapi produsen. Salah satu kendala utama adalah persyaratan bagi produsen asing untuk bekerja sama dengan importir lokal berlisensi untuk mengajukan permohonan pendaftaran. Peran perantara ini dapat menambah biaya dan kompleksitas proses. Keterlibatan perwakilan lokal memastikan kepatuhan terhadap peraturan setempat. Hal ini memudahkan komunikasi dengan Kementerian Kesehatan, tetapi juga dapat menyebabkan penundaan jika pemahaman importir tentang persyaratan peraturan kurang atau koordinasi yang tidak memadai antara pihak-pihak yang terlibat. Komunikasi dengan Kementerian Kesehatan merupakan tantangan penting lainnya. Proses regulasi dapat melibatkan beberapa interaksi yang memerlukan informasi tambahan atau koreksi. Hal ini dapat menjadi hambatan jika dokumentasi yang diserahkan tidak lengkap atau terdapat ambiguitas dalam data yang diberikan. Sifat iteratif dari proses komunikasi dapat menunda jangka waktu pendaftaran, yang berdampak pada ketersediaan alat kesehatan di pasar. Lebih lanjut, kerangka regulasi di Indonesia bersifat dinamis, dengan pembaruan yang berkelanjutan, seperti penerapan persyaratan sertifikasi Halal untuk alat kesehatan. Produsen harus tetap waspada dan mendapatkan informasi terbaru tentang setiap perubahan pada lanskap regulasi untuk memastikan produk mereka tetap patuh. Agar dapat mengikuti perkembangan terbaru ini diperlukan keterlibatan aktif dengan Kementerian Kesehatan dan manajemen proaktif terhadap portofolio regulasi, yang dapat memerlukan banyak sumber daya, terutama bagi perusahaan asing yang tidak terbiasa dengan lingkungan regulasi lokal.
Kesimpulan
Sebagai kesimpulan, klasifikasi alat kesehatan di Indonesia mengikuti kerangka kerja terstruktur yang selaras dengan standar global, khususnya pedoman Global Harmonization Task Force (GHTF), dan diselaraskan dengan ASEAN Medical Devices Directive (AMDD). Klasifikasi Kelas I, II, dan III menentukan tingkat risiko yang ditimbulkan perangkat terhadap pasien dan pengguna, yang memengaruhi proses registrasi, pengawasan regulasi, dan biaya terkait. Setiap kelas memiliki kriteria dan persyaratan regulasi yang berbeda, mulai dari dokumentasi minimal untuk perangkat Kelas I hingga evaluasi komprehensif untuk perangkat Kelas III, termasuk uji klinis dan pengujian biokompatibilitas. Pengenalan e-Katalog semakin menyederhanakan pengadaan, meningkatkan transparansi dan efisiensi. Menavigasi klasifikasi dan proses registrasi ini memerlukan pemahaman yang mendalam tentang lanskap regulasi dan tuntutan spesifik dari sistem e-Katalog, yang sangat penting bagi produsen yang ingin sukses di pasar Indonesia.





